ST2STL Ch1-La Sécurité Routière
Prévenir et Sécuriser
Ajouter à mes favoris
La sécurité routière PARTIE 1
| Notions et contenus |
Connaissances et capacités exigibles
Activités expérimentales support de la formation |
Comment une transformation chimique permet-elle de gonfler un airbag /coussin gonflable ?
|
Bilan de matière
Volume molaire Vm . |
Mettre en œuvre un protocole de mesure d’un volume de gaz produit lors d’une transformation chimique.
Faire un bilan de matière à partir d’une équation de réaction fournie. Utiliser la relation V = n × Vm . S’approprier et analyser des informations pour expliquer le fonctionnement d’un airbag. |
I - Comment une transformation chimique permet-elle de gonfler un airbag /coussin gonflable
?
Objectif :
Comparer le résultat d’une expérience avec un résultat théorique.
Dans cette activité, vous allez déterminer le volume d’un gaz formé lors d’une réaction chimique.
Des résultats d’expériences vous seront présentés et devront être analysés.
Rappels
outils

1 - Activité expérimentale : Comment déterminer le volume d'un gaz produit lors d'une transformation chimique ?

Produire du gaz expérimentalement
Ci-contre e schéma montre comment recueillir un gaz par déplacement d'eau.
Le principe de recueillir un gaz par
déplacement d'eau
.
La boisson pétillante est versée dans un ballon qui est placé dans un chauffe-ballon. On chauffe légèrement la boisson (sans provoquer l'ébullition) afin de favoriser le dégagement du
gaz
: l'élévation de température diminue la solubilité des
gaz
.
Le protocole du document 3 de l'activité 1 page 14 du livre est
réalisé suivant la vidéo ci-contre :
Après avoir visualiser la vidéo répondre aux questions
de la page 14 de votre livre.
Voici une expérience permettant de déterminer le volume de gaz formé :
À l’aide d’une burette, on introduit un excès d’acide chlorhydrique dans un erlenmeyer contenant une masse de m = 84 mg d’hydrogénocarbonate de sodium (montage A). Il se forme un gaz qui s’échappe grâce au tube de dégagement dans une éprouvette contenant de l’eau distillée (Montage B).
Le gaz va remplacer l’eau contenue dans l’éprouvette et on pourra ainsi déterminer le volume de gaz formé.
Équation bilan de l’expérience :
En A : acide chlorhydrique (liquide) + hydrogénocarbonate de sodium (solide)
En B : eau + sodium + chlore + dioxyde de carbone
(H+ + Cl- ) (aq) + NaHCO3 (s) → H2O(l) + CO2 (g)+ Na+ (aq) + Cl- (aq)
Voici ci-contre le schéma de l’expérience

Question 1 : Associer à chaque numéro, le nom de la verrerie en vous servant du descriptif.
|
Cristallisoir
|
|
Burette
|
|
|
Potence
|
|
Éprouvette
|
|
|
Erlenmeyer
|
|
Tube à dégagement |
|
Question 2 et 3
: Cocher les bonnes réponses :
|
|
Réactifs
|
Produits | gaz | liquide | solide |
|
Dioxyde de carbone
|
|
|
|
|
|
|
Hydrogénocarbonate de sodium
|
|
|
|
|
|
|
Acide chlorhydrique
|
|
|
|
|
|
|
Eau
|
|
|
|
|
|
2. Détermination de la quantité de matière de gaz formé théorique
On peut prévoir théoriquement la quantité de matière de gaz qui va se former en utilisant l’équation de la réaction.
On détermine dans un premier temps la quantité de matière (n) d’hydrogénocarbonate de sodium introduit car c’est le réactif en défaut donc limitant et il va être totalement consommé.
Masse molaire moléculaire : C’est la somme des masses molaires atomiques des atomes constituants une molécule ou un ion.
Ex : l’eau H 2 0 M( H 2 0) = 2 x M (H) + 1 x M (O) = 2x1+1x16 = 18 g.mol -1
en utilisant M (C) = 12 g.mol -1 ; M (O) = 16 g.mol -1 ; M (H) = 1 g.mol -1 ; M (Na) = 23 g.mol -1 ; M(N) = 14 g.mol -1
La quantité de matière n : s’exprime en mole (unité mol) et se calcule par la relation : n = m / M
Question 4 : Retrouver la masse molaire moléculaire de l’hydrogénocarbonate de sodium :
- M = 84 g.mol -1
- M = 61 g.mol -1
Question 5
: Retrouver la valeur de la quantité de matière d’hydrogénocarbonate de sodium (HCO3Na).
-
n = 0,001 mol
-
n = 0,85 mol
-
n = 0,01 g
L’équation bilan nous montre qu’une mole d’hydrogénocarbonate de sodium donne une mole de dioxyde de carbone:
(H+ (aq) + Cl- (aq) )+ 1NaHCO3 (s) → H2O(l) + 1CO2 (g)+ Na+ (aq)+ Cl- (aq)
On peut donc en déduire que n(CO2) = n(NaHCO3)
Question 6 : Retrouver la valeur de la quantité de matière de dioxyde de carbone.
On constate qu’……….mol d’hydrogénocarbonate de sodium réagit pour donner une mole de ……………. (CO2).
- n = 0,001 mol
- n = 1 mol
- n = 44 mol
3. Détermination du volume de gaz
Volume molaire
V
m
C’est le volume occupé par une mole de gaz, dans des conditions données, il est indépendant de la nature du gaz. Le volume molaire est le rapport du volume de gaz par le nombre de mole qu’il contient. On le note Vm et s’exprime en L.mol
–1
.
Les gaz ont une propriété particulière : dans les mêmes conditions de pression et de températures, une quantité de matière n de gaz occupe le même volume V quelque soit le gaz. Le volume occupé par une mole de gaz, noté V m , est appelé volume molaire. Son unité est le L.mol –1 .

Résumé
|
La réaction chimique entre l'acide chlorhydrique et le magnésium produit un gaz qu'on peut recueillir par déplacement d'eau . Il s'agit d'une réaction d'oxydoréduction mettant en jeu les 2 couples Mg2+/Mg et H+/H2 les 2 réactifs : le magnésium solide Mg qui est le réducteur et les ions H+ oxydant réagissent pour donner l'ion Mg 2+ et le gaz H2. Il y a transfert de 2 électrons de Mg(s) vers H+(aq)
Le volume du gaz recueilli V est donné par la formule V = n x Vm Les coefficients stoechiométriques pour le magnésium utilisé et le gaz obtenu sont les mêmes donc on a la même quantité de matière n selon l'outil 1 on peut calculer aisément n = m/M puis V. 
|
|
Q
ue retenir de cette activité ?
La quantité de gaz produite lors d’une réaction chimique peut être mesurée expérimentalement. On la détermine par lecture du volume au niveau de l’éprouvette dans ce cas. Le volume peut être déterminé théoriquement en utilisant la définition du volume molaire. Il faut utiliser les coefficients stœchiométriques de l’équation bilan de la réaction pour déterminer la quantité de matière du gaz. Ces coefficients expriment le nombre de moles intervenant et rendent compte de la proportionnalité entre les réactifs qui disparaissent et entre les produits formés selon la loi de Lavoisier : « rien ne se perd, rien ne se crée, tout se transforme » |
1. principe de fonctionnement de l'airbag
L’airbag ou coussin est un accessoire de sécurité passive développé pour l’automobile à la fin des années 1980 et qui équipe maintenant toutes les automobiles. C’est un sac qui se remplit de gaz pour amortir les chocs en cas d'accident. c'est grâce à une réaction chimique se produisant dans un générateur de gaz relié au coussin gonflable que se réalise le déploiement de l’airbag. Ce gaz doit être inerte, ni toxique, ni combustible ou comburant d'où le choix porté sur le diazote N2.
Ce générateur de gaz contient des pastilles blanches constituées d’azoture de sodium, espèce chimique de formule NaN3(s) qui se décompose très rapidement et libère ainsi une quantité suffisante de gaz pour déployer l’airbag en cas de choc. (elles contiennent aussi du nitrate de potassium (KNO3) et de la silice (SiO2).
La durée entre le choc et le gonflage du ballon n’est que de 40 millisecondes, d’où l’intérêt de ce mécanisme.
Plusieurs réactions se produisent à la suite de l'amorçage du détonateur, toutes les espèces sont solides sauf le diazote (voir doc 3 page 15 du livre)
L’équation de la réaction chimique est la suivante : 2 NaN3(s) → 2 Na(s) + 3 N2(g)
Question 7 : Pour chaque proposition ci-dessous, cocher VRAI ou FAUX
|
|
VRAI
|
FAUX
|
|
Le gaz qui se forme est le diazote
|
|
|
|
Le gaz qui se forme est l’azoture de sodium
|
|
|
|
Le gaz qui se forme est le sodium
|
|
|
Compléter :
| NaN3 | Na | N2 | KNO3 | K2O et Na2O | SiO2 | K2Na2SiO4 | Na4SiO4 |
|
|
|
|
|
|
|
|
|
Résumé
|
Le principe de l'airbag est de se gonfler très rapidement pour protéger les passagers en cas de choc.
Le choc entraine le déclenchement d'une suite de réaction chimique explosive dont l'un des produits est le gaz servant à gonfler l'airbag. Par suite il faut éliminer tous les autres éléments dangereux produits intervenant dans le processus |
A retenir
- Masse molaire moléculaire :
C’est la somme des masses molaires atomiques des atomes constituants une molécule ou un ion.
- La quantité de matière n :
s’exprime en mol et se calcule par la relation suivante ; n = m / M tout en sachant que m(g) est la masse quelconque d’un composé prélevé à l’aide d’une balance.
— L’équation bilan nous montre qu’une mole d’hydrogénocarbonate de sodium donne une mole de dioxyde de carbone :
(H+ (aq) + Cl- (aq))+ 1 NaHCO3 (s) → H2O(l) + 1 CO2 (g)+ Na+ (aq)+ Cl- (aq)
On peut donc en déduire que n(CO2) = n(NaHCO3)
- Volume molaire :
C’est le volume occupé par une mole de gaz, dans des conditions données de température et de pression, il est indépendant de la nature du gaz. Le volume molaire est le rapport du volume de gaz par le nombre de mole qu’il contient. On le note Vm et s’exprime en L.mol-1
V=Vm x n
Dans les mêmes conditions de température et de pression tous les gaz ont le même volume molaire.
Vm= 22,4 L.mol-1 à T= 0°C , P= 1,013 x 105 Pa dites conditions normales de température et de pression ou CNTP.
Vm= 24 L.mol-1 à T= 25°C , P= 1,013 x 105 Pa dites conditions standards de température et de pression ou CSTP.
— Les réactions d’oxydo-réduction échangent des électrons entre espèces chimiques :
Un oxydan t est une espèce chimique capable de capter un ou plusieurs électrons.
Un réducteur est une espèce chimique capable de céder un ou plusieurs électrons.
Un oxydant et un réducteur forment un couple Oxydant/Réducteur, noté Ox/Red Ils sont liés par la demi-équation électronique :
Ox + n e- = Red
• Dans le sens : Ox + n e- → Red C’est une réduction (gain d’électrons)
• Dans le sens : Red → n e- + Ox C’est une oxydation (perte d’électrons)
Méthode de compréhension d’écriture des demi-équations :
• Ecrire le couple : Ox/Red puis Ox + n e- = Red
• Equilibrer les atomes autres que l’oxygène et l’hydrogène
• Equilibrer les oxygènes avec de l’eau (H2O)
• Equilibrer les hydrogènes avec des protons (H+ )
• Equilibrer les charges en ajoutant des électrons (e- ) du côté de l’oxydant
Exemples :
Fe3+ / Fe2+ : Fe3+ + 1 e- = Fe2+
ClO- / Cl2 : 2ClO- + 4H+ + 4 e- = Cl2 + 2 H2O
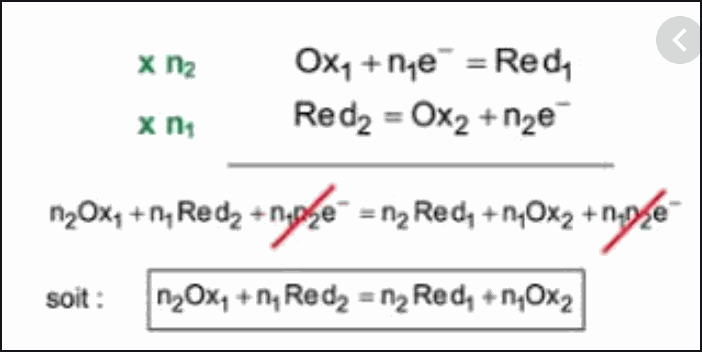
Méthode d’écriture de l’équation bilan, exigible :
• Repérer dans chaque couple, quel oxydant réagit avec quel réducteur (bien lire l’énoncé)
• Ecrire les demi-équations de chaque couple dans le bon sens (Réactifs à gauche, Produits à droite)
• Equilibrer les deux demi-équations en faisant attention à ce que le nombre d’électrons échangés soit le même dans les deux demi-équations de réaction
• Additionner les deux demi-équations afin d’obtenir l’équation bilan (il ne doit pas rester d’électrons)
exemple :


Laisser un commentaire
Vous devez être Connecté en tant que pour poster un commentaire.